Обусловлены действием ангиотензина ii. Сартаны: действие, применение, перечень препаратов, показания и противопоказания
Препараты подгрупп исключены . Включить
Описание
Антагонисты рецепторов ангиотензина II, или блокаторы АТ 1 -рецепторов — одна из новых групп антигипертензивных средств. Она объединяет лекарственные средства, модулирующие функционирование ренин-ангиотензин-альдостероновой системы (РААС ) посредством взаимодействия с ангиотензиновыми рецепторами.
РААС играет важную роль в регуляции АД , патогенезе артериальной гипертензии и хронической сердечной недостаточности (ХСН ) , а также ряда других заболеваний. Ангиотензины (от angio — сосудистый и tensio — напряжение) — пептиды, образующиеся в организме из ангиотензиногена, представляющего собой гликопротеид (альфа 2 -глобулин) плазмы крови, синтезирующийся в печени. Под воздействием ренина (фермент, образующийся в юкстагломерулярном аппарате почек) полипептид ангиотензиноген, не обладающий прессорной активностью, гидролизуется, образуя ангиотензин I — биологически неактивный декапептид, легко подвергающийся дальнейшим преобразованиям. Под действием ангиотензинпревращающего фермента (АПФ ) , образующегося в легких, ангиотензин I превращается в октапептид — ангиотензин II, являющийся высокоактивным эндогенным прессорным соединением.
Ангиотензин II — основной эффекторный пептид РААС . Он оказывает сильное сосудосуживающее действие, повышает ОПСС , вызывает быстрое повышение АД . Кроме того, он стимулирует секрецию альдостерона, а в больших концентрациях — увеличивает секрецию антидиуретического гормона (повышение реабсорбции натрия и воды, гиперволемия) и вызывает симпатическую активацию. Все эти эффекты способствуют развитию гипертензии.
Ангиотензин II быстро метаболизируется (период полураспада — 12 мин) при участии аминопептидазы А с образованием ангиотензина III и далее под влиянием аминопептидазы N — ангиотензина IV, обладающих биологической активностью. Ангиотензин III стимулирует выработку альдостерона надпочечниками, обладает положительной инотропной активностью. Ангиотензин IV, предположительно, участвует в регуляции гемостаза.
Известно, что помимо РААС системного кровотока, активация которой приводит к краткосрочным эффектам (в т.ч. таким как вазоконстрикция, повышение АД , секреция альдостерона), имеются локальные (тканевые) РААС в различных органах и тканях, в т.ч. в сердце, почках, мозге, кровеносных сосудах. Повышенная активность тканевых РААС обусловливает долговременные эффекты ангиотензина II, которые проявляются структурно-функциональными изменениями в органах-мишенях и приводят к развитию таких патологических процессов, как гипертрофия миокарда, миофиброз, атеросклеротическое поражение сосудов мозга, поражение почек и др.
В настоящее время показано, что у человека, помимо АПФ-зависимого пути преобразования ангиотензина I в ангиотензин II, существуют альтернативные пути — с участием химаз, катепсина G, тонина и др. сериновых протеаз. Химазы, или химотрипсиноподобные протеазы, представляют собой гликопротеины с молекулярной массой около 30000. Химазы имеют высокую специфичность по отношению к ангиотензину I. В разных органах и тканях преобладает либо АПФ-зависимый, либо альтернативные пути образования ангиотензина II. Так, в ткани миокарда человека обнаружена кардиальная серинпротеаза, ее ДНК и мРНК. При этом наибольшее количество этого фермента содержится в миокарде левого желудочка, где на долю химазного пути приходится более 80%. Химазозависимое образование ангиотензина II превалирует в миокардиальном интерстиции, адвентиции и медии сосудов, тогда как АПФ-зависимое — в плазме крови.
Ангиотензин II может формироваться и непосредственно из ангиотензиногена путем реакций, катализируемых тканевым активатором плазминогена, тонином, катепсином G и др.
Полагают, что активация альтернативных путей образования ангиотензина II играет большую роль в процессах сердечно-сосудистого ремоделирования.
Физиологические эффекты ангиотензина II, как и других биологически активных ангиотензинов, реализуются на клеточном уровне через специфические ангиотензиновые рецепторы.
К настоящему времени установлено существование нескольких подтипов ангиотензиновых рецепторов: АТ 1 , АТ 2 , АТ 3 и АТ 4 и др.
У человека идентифицированы и наиболее полно изучены два подтипа мембраносвязанных, сопряженных с G-белком рецепторов ангиотензина II — подтипы АТ 1 и АТ 2 .
АТ 1 -рецепторы локализуются в различных органах и тканях, преимущественно в гладкой мускулатуре сосудов, сердце, печени, коре надпочечников, почках, легких, в некоторых областях мозга.
Большинство физиологических эффектов ангиотензина II, включая и неблагоприятные, опосредуется АТ 1 -рецепторами:
Артериальная вазоконстрикция, в т.ч. вазоконстрикция артериол почечных клубочков (особенно выносящих), повышение гидравлического давления в почечных клубочках,
Усиление реабсорбции натрия в проксимальных почечных канальцах,
Секреция альдостерона корой надпочечников,
Секреция вазопрессина, эндотелина−1,
Высвобождение ренина,
Усиление высвобождения норадреналина из симпатических нервных окончаний, активация симпатико-адреналовой системы,
Пролиферация гладкомышечных клеток сосудов, гиперплазия интимы, гипертрофия кардиомиоцитов, стимуляция процессов ремоделирования сосудов и сердца.
При артериальной гипертензии на фоне чрезмерной активации РААС опосредуемые АТ 1 -рецепторами эффекты ангиотензина II прямо или косвенно способствуют повышению АД . Кроме того, стимуляция этих рецепторов сопровождается повреждающим действием ангиотензина II на сердечно-сосудистую систему, включая развитие гипертрофии миокарда, утолщение стенок артерий и др.
Эффекты ангиотензина II, опосредуемые АТ 2 -рецепторами, были обнаружены лишь в последние годы.
Большое количество АТ 2 -рецепторов обнаружено в тканях плода (в т.ч. и в мозге). В постнатальном периоде количество АТ 2 -рецепторов в тканях человека уменьшается. Экспериментальные исследования, в частности у мышей, у которых был разрушен ген, кодирующий АТ 2 -рецепторы, позволяют предположить их участие в процессах роста и созревания, включая пролиферацию и дифференцировку клеток, развитие эмбриональных тканей, а также формирование исследовательского поведения.
АТ 2 -рецепторы найдены в сердце, сосудах, надпочечниках, почках, некоторых областях мозга, репродуктивных органах, в т.ч. в матке, атрезированных фолликулах яичников, а также в ранах кожи. Показано, что количество АТ 2 -рецепторов может увеличиваться при повреждении тканей (в т.ч. сосудов), инфаркте миокарда, сердечной недостаточности. Предполагают, что эти рецепторы могут быть вовлечены в процессы регенерации тканей и программированной гибели клеток (апоптоз).
Исследования последних лет показывают, что кардиоваскулярные эффекты ангиотензина II, опосредованные АТ 2 -рецепторами, противоположны эффектам, обусловленным возбуждением АТ 1 -рецепторов, и являются относительно слабо выраженными. Стимуляция АТ 2 -рецепторов сопровождается вазодилатацией, ингибированием клеточного роста, в т.ч. подавлением пролиферации клеток (эндотелиальных и гладкомышечных клеток сосудистой стенки, фибробластов и др.), торможением гипертрофии кардиомиоцитов.
Физиологическая роль рецепторов ангиотензина II второго типа (АТ 2) у человека и их связь с кардиоваскулярным гомеостазом в настоящее время до конца не выяснены.
Синтезированы высокоселективные антагонисты АТ 2 -рецепторов (CGP 42112А, PD 123177, PD 123319), которые используются в экспериментальных исследованиях РААС .
Другие ангиотензиновые рецепторы и их роль в организме человека и животных мало изучены.
Из клеточной культуры мезангия крыс выделены подтипы АТ 1 -рецепторов — АТ 1а и АТ 1b , различающиеся аффинностью к пептидным агонистам ангиотензина II (у человека эти подтипы не обнаружены). Из плаценты крыс выделен АТ 1с -подтип рецепторов, физиологическая роль которого пока не ясна.
АТ 3 -рецепторы, обладающие сродством к ангиотензину II, обнаружены на мембранах нейронов, функция их неизвестна. АТ 4 -рецепторы найдены на эндотелиальных клетках. Взаимодействуя с этими рецепторами, ангиотензин IV стимулирует высвобождение из эндотелия ингибитора активатора плазминогена 1-го типа. АТ 4 -рецепторы обнаружены также на мембранах нейронов, в т.ч. в гипоталамусе, предположительно, в мозге они опосредуют познавательные функции. Тропностью к АТ 4 -рецепторам обладает, кроме ангиотензина IV, также ангиотензин III.
Многолетние исследования РААС не только выявили важное значение этой системы в регуляции гомеостаза, в развитии сердечно-сосудистой патологии, влиянии на функции органов-мишеней, среди которых наиболее важными являются сердце, кровеносные сосуды, почки и мозг, но и привели к созданию лекарственных средств, целенаправленно действующих на отдельные звенья РААС .
Научной основой создания лекарственных средств, действующих путем блокады ангиотензиновых рецепторов, явилось изучение ингибиторов ангиотензина II. Экспериментальные исследования показывают, что антагонистами ангиотензина II, способными блокировать его образование или действие и понизить таким образом активность РААС , являются ингибиторы образования ангиотензиногена, ингибиторы синтеза ренина, ингибиторы образования или активности АПФ , антитела, антагонисты ангиотензиновых рецепторов, в том числе синтетические непептидные соединения, специфически блокирующие АТ 1 -рецепторы, и др.
Первым блокатором рецепторов ангиотензина II, внедренным в терапевтическую практику в 1971 г., был саралазин — пептидное соединение, близкое по структуре к ангиотензину II. Саралазин блокировал прессорное действие ангиотензина II и понижал тонус периферических сосудов, уменьшал содержание альдостерона в плазме, понижал АД . Однако к середине 70-х годов опыт применения саралазина показал, что он обладает свойствами частичного агониста и в ряде случаев дает плохо прогнозируемый эффект (в виде чрезмерной гипотензии или гипертензии). При этом хороший гипотензивный эффект проявлялся при состояниях, сопряженных с высоким уровнем ренина, тогда как на фоне низкого уровня ангиотензина II или при быстрой инъекции АД повышалось. В связи с наличием агонистических свойств, а также ввиду сложности синтеза и необходимости парентерального введения широкого практического применения саралазин не получил.
В начале 90-х годов был синтезирован первый непептидный селективный антагонист АТ 1 -рецепторов, эффективный при приеме внутрь — лозартан, получивший практическое применение в качестве антигипертензивного средства.
В настоящее время в мировой лечебной практике применяются или проходят клинические испытания несколько синтетических непептидных селективных АТ 1 -блокаторов — валсартан, ирбесартан, кандесартан, лозартан, телмисартан, эпросартан, олмесартана медоксомил, азилсартана медоксомил, золарсартан, тазосартан (золарсартан и тазосартан пока не зарегистрированы в России).
Существует несколько классификаций антагонистов рецепторов ангиотензина II: по химической структуре, фармакокинетическим особенностям, механизму связывания с рецепторами и др.
По химической структуре непептидные блокаторы АТ 1 -рецепторов можно разделить на 3 основные группы:
Бифениловые производные тетразола: лозартан, ирбесартан, кандесартан, валсартан, тазосартан;
Бифениловые нететразоловые соединения — телмисартан;
Небифениловые нететразоловые соединения — эпросартан.
По наличию фармакологической активности блокаторы АТ 1 -рецепторов делят на активные лекарственные формы и пролекарства. Так, валсартан, ирбесартан, телмисартан, эпросартан сами обладают фармакологической активностью, тогда как кандесартана цилексетил становится активным лишь после метаболических превращений в печени.
Кроме того, АТ 1 -блокаторы различаются в зависимости от наличия или отсутствия у них активных метаболитов. Активные метаболиты имеются у лозартана и тазосартана. Например, активный метаболит лозартана — EXP−3174 оказывает более сильное и длительное действие, чем лозартан (по фармакологической активности EXP−3174 превосходит лозартан в 10-40 раз).
По механизму связывания с рецепторами блокаторы АТ 1 -рецепторов (а также их активные метаболиты) делят на конкурентные и неконкурентные антагонисты ангиотензина II. Так, лозартан и эпросартан обратимо связываются с АТ 1 -рецепторами и являются конкурентыми антагонистами (т.е. при определенных условиях, например, при повышении уровня ангиотензина II в ответ на уменьшение ОЦК , могут вытесняться из мест связывания), тогда как валсартан, ирбесартан, кандесартан, телмисартан, а также активный метаболит лозартана EXP−3174 действуют как неконкурентные антагонисты и связываются с рецепторами необратимо.
Фармакологическое действие средств этой группы обусловлено устранением сердечно-сосудистых эффектов ангиотензина II, в т.ч. вазопрессорного.
Полагают, что антигипертензивное действие и другие фармакологические эффекты антагонистов рецепторов ангиотензина II реализуются несколькими путями (один прямой и несколько опосредованных).
Основной механизм действия лекарственных средств этой группы связан с блокадой АТ 1 -рецепторов. Все они являются высокоселективными антагонистами АТ 1 -рецепторов. Показано, что их аффинность к АТ 1 - превышает таковую к АТ 2 -рецепторам в тысячи раз: для лозартана и эпросартана более чем в 1 тыс. раз, телмисартана — более 3 тыс., ирбесартана — 8,5 тыс., активного метаболита лозартана EXP−3174 и кандесартана — 10 тыс., олмесартана - в 12,5 тыс., валсартана — в 20 тыс. раз.
Блокада АТ 1 -рецепторов препятствует развитию эффектов ангиотензина II, опосредуемых этими рецепторами, что предотвращает неблагоприятное влияние ангиотензина II на сосудистый тонус и сопровождается снижением повышенного АД . Длительный прием этих лекарственных средств приводит к ослаблению пролиферативных эффектов ангиотензина II в отношении гладкомышечных клеток сосудов, мезангиальных клеток, фибробластов, уменьшению гипертрофии кардиомиоцитов и др.
Известно, что АТ 1 -рецепторы клеток юкстагломерулярного аппарата почек вовлечены в процесс регуляции высвобождения ренина (по принципу отрицательной обратной связи). Блокада АТ 1 -рецепторов вызывает компенсаторное увеличение активности ренина, повышение продукции ангиотензина I, ангиотензина II и др.
В условиях повышенного содержания ангиотензина II на фоне блокады АТ 1 -рецепторов проявляются защитные свойства этого пептида, реализующиеся посредством стимуляции АТ 2 -рецепторов и выражающиеся в вазодилатации, замедлении пролиферативных процессов и др.
Кроме того, на фоне повышенного уровня ангиотензинов I и II происходит образование ангиотензина-(1-7). Ангиотензин-(1-7) образуется из ангиотензина I под действием нейтральной эндопептидазы и из ангиотензина II под действием пролиловой эндопептидазы и является еще одним эффекторным пептидом РААС , оказывающим вазодилатирующее и натрийуретическое действие. Эффекты ангиотензина-(1-7) опосредованы через так называемые, не идентифицированные пока, АТ x рецепторы.
Недавние исследования дисфункции эндотелия при артериальной гипертензии позволяют предположить, что кардиоваскулярные эффекты блокаторов ангиотензиновых рецепторов могут быть также связаны с модуляцией эндотелия и влиянием на продукцию оксида азота (NO). Полученные экспериментальные данные и результаты отдельных клинических исследований достаточно противоречивы. Возможно, на фоне блокады АТ 1 -рецепторов, увеличивается эндотелийзависимый синтез и высвобождение оксида азота, что способствует вазодилатации, уменьшению агрегации тромбоцитов и снижению пролиферации клеток.
Таким образом, специфическая блокада АТ 1 -рецепторов позволяет обеспечить выраженный антигипертензивный и органопротективный эффект. На фоне блокады АТ 1 -рецепторов тормозится неблагоприятное воздействие ангиотензина II (и ангиотензина III, обладающего сродством к рецепторам ангиотензина II) на сердечно-сосудистую систему и, предположительно, проявляется его защитное действие (путем стимуляции АТ 2 -рецепторов), а также развивается действие ангиотензина-(1-7) путем стимуляции АТ x -рецепторов. Все эти эффекты способствуют вазодилатации и ослаблению пролиферативного действия ангиотензина II в отношении клеток сосудов и сердца.
Антагонисты АТ 1 -рецепторов могут проникать через гематоэнцефалический барьер и тормозить активность медиаторных процессов в симпатической нервной системе. Блокируя пресинаптические АТ 1 -рецепторы симпатических нейронов в ЦНС , они угнетают высвобождение норадреналина и уменьшают стимуляцию адренорецепторов гладкой мускулатуры сосудов, что приводит к вазодилатации. Экспериментальные исследования показывают, что этот дополнительный механизм вазодилатирующего действия более характерен для эпросартана. Данные о действии лозартана, ирбесартана, валсартана и др. на симпатическую нервную систему (которое проявлялось при дозах, превышающих терапевтические) весьма противоречивы.
Все блокаторы рецепторов АТ 1 действуют постепенно, антигипертензивный эффект развивается плавно, в течение нескольких часов после приема однократной дозы, и продолжается до 24 ч. При регулярном применении выраженный терапевтический эффект обычно достигается через 2-4 нед (до 6 нед) лечения.
Особенности фармакокинетики средств этой группы делают удобным их применение пациентами. Эти лекарственные средства можно принимать вне зависимости от приема пищи. Однократного приема достаточно, чтобы обеспечить хороший гипотензивный эффект в течение суток. Они одинаково эффективны у больных разного пола и возраста, включая пациентов старше 65 лет.
Клинические исследования показывают, что все блокаторы ангиотензиновых рецепторов обладают высоким антигипертензивным и выраженным органопротективным эффектом, хорошей переносимостью. Это позволяет использовать их, наряду с другими гипотензивными средствами, для лечения больных с сердечно-сосудистой патологией.
Основным показанием для клинического применения блокаторов рецепторов ангиотензина II является лечение артериальной гипертензии различной степени выраженности. Возможна монотерапия (при мягкой артериальной гипертензии) или в комбинации с другими гипотензивными средствами (при умеренной и тяжелой формах).
В настоящее время по рекомендациям ВОЗ/МОГ (Международного общества по гипертензии) предпочтение отдается комбинированной терапии. Наиболее рациональной для антагонистов рецепторов ангиотензина II является их комбинация с тиазидными диуретиками. Добавление диуретика в низких дозах (например, 12,5 мг гидрохлоротиазида) позволяет повысить эффективность терапии, что подтверждается результатами рандомизированных мультицентровых исследований. Созданы препараты, в состав которых входит эта комбинация — Гизаар (лозартан + гидрохлоротиазид), Ко-диован (валсартан + гидрохлоротиазид), Коапровель (ирбесартан + гидрохлоротиазид), Атаканд Плюс (кандесартан + гидрохлоротиазид), Микардис Плюс (телмисартан + гидрохлоротиазид) и др.
В ряде многоцентровых исследований (ELITE, ELITE II, Val-HeFT и др.) показана эффективность применения некоторых антагонистов АТ 1 -рецепторов при ХСН . Результаты этих исследований неоднозначны, но в целом они свидетельствуют о высокой эффективности и лучшей (по сравнению с ингибиторами АПФ) переносимости.
Результаты экспериментальных, а также клинических исследований свидетельствуют, что блокаторы рецепторов АТ 1 -подтипа не только предотвращают процессы сердечно-сосудистого ремоделирования, но и вызывают обратное развитие гипертрофии левого желудочка (ГЛЖ). В частности показано, что при длительной терапии лозартаном у больных отмечалась тенденция к уменьшению размеров левого желудочка в систолу и диастолу, повышение сократимости миокарда. Регрессия ГЛЖ была отмечена при длительном применении валсартана и эпросартана у больных артериальной гипертензией. У некоторых блокаторов рецепторов подтипа АТ 1 обнаружена способность улучшать почечную функцию, в т.ч. при диабетической нефропатии, а также показатели центральной гемодинамики при ХСН . Пока клинические наблюдения, касающиеся влияния этих средств на органы-мишени немногочисленны, но исследования в этой области активно продолжаются.
Противопоказаниями к применению блокаторов ангиотензиновых АТ 1 -рецепторов являются индивидуальная гиперчувствительность, беременность, кормление грудью.
Данные, полученные в экспериментах на животных, свидетельствуют, что средства, оказывающие прямое действие на РААС , могут вызывать повреждения у плода, смерть плода и новорожденного. Особенно опасно воздействие на плод во II и III триместрах беременности, т.к. возможно развитие гипотензии, гипоплазии черепа, анурии, почечной недостаточности и летального исхода у плода. Прямые указания на развитие подобных дефектов при приеме блокаторов АТ 1 -рецепторов отсутствуют, однако средства этой группы не следует применять в период беременности, а при выявлении беременности в период лечения их прием необходимо прекратить.
Отсутствуют сведения о способности блокаторов АТ 1 -рецепторов проникать в грудное молоко женщин. Однако в экспериментах на животных установлено, что они проникают в молоко лактирующих крыс (в молоке крыс обнаруживаются значительные концентрации не только самих веществ, но и их активных метаболитов). В связи с этим блокаторы АТ 1 -рецепторов не применяют у кормящих женщин, а в случае необходимости терапии для матери прекращают кормление грудью.
Следует воздерживаться от использования этих лекарственных средств в педиатрической практике, поскольку безопасность и эффективность их применения у детей не определены.
Для терапии антагонистами АТ 1 ангиотензиновых рецепторов существует ряд ограничений. Осторожность следует проявлять у больных с пониженным ОЦК и/или гипонатриемией (при лечении диуретиками, ограничении поступления соли с диетой, диарее, рвоте), а также у пациентов, находящихся на гемодиализе, т.к. возможно развитие симптоматической гипотензии. Оценка соотношения риск/польза необходима у больных с реноваскулярной гипертензией, обусловленной двусторонним стенозом почечных артерий или стенозом почечной артерии единственной почки, т.к. чрезмерное угнетение РААС в этих случаях повышает риск развития тяжелой гипотензии и почечной недостаточности. С осторожностью следует применять при аортальном или митральном стенозе, обструктивной гипертрофической кардиомиопатии. На фоне нарушения функции почек необходим мониторинг уровней калия и креатинина сыворотки. Не рекомендуется применять пациентам с первичным гиперальдостеронизмом, т.к. в этом случае лекарственные средства, угнетающие РААС , неэффективны. Отсутствуют достаточные данные о применении у больных с тяжелыми заболеваниями печени (например, при циррозе).
Побочные эффекты при приеме антагонистов рецепторов ангиотензина II, о которых до сих пор сообщалось, обычно мало выражены, носят преходящий характер и редко являются основанием для отмены терапии. Суммарная частота побочных эффектов сравнима с плацебо, что подтверждается результатами плацебо-контролируемых исследований. Наиболее частыми неблагоприятными эффектами являются головная боль, головокружение, общая слабость и др. Антагонисты ангиотензиновых рецепторов не оказывают прямого влияния на метаболизм брадикинина, субстанции Р, других пептидов и вследствие этого не вызывают сухого кашля, нередко появляющегося при лечении ингибиторами АПФ .
При приеме лекарственных средств этой группы отсутствует эффект гипотензии первой дозы, встречающийся при приеме ингибиторов АПФ , а внезапная отмена не сопровождается развитием рикошетной гипертензии.
Результаты мультицентровых плацебо-контролируемых исследований показывают высокую эффективность и хорошую переносимость антагонистов АТ 1 -рецепторов ангиотензина II. Однако пока их использование ограничивается отсутствием данных об отдаленных последствиях применения. По мнению экспертов ВОЗ/МОГ, их применение для лечения артериальной гипертензии целесообразно при непереносимости ингибиторов АПФ , в частности, в случае указания на кашель в анамнезе, вызываемый ингибиторами АПФ .
В настоящее время продолжаются многочисленные клинические исследования, в т.ч. и мультицентровые, посвященные изучению эффективности и безопасности применения антагонистов рецепторов ангиотензина II, их влияния на смертность, продолжительность и качество жизни больных и сравнению с гипотензивными и др. средствами при лечении артериальной гипертензии, хронической сердечной недостаточности, атеросклероза и др.
Препараты
Препаратов - 4133 ; Торговых названий - 84 ; Действующих веществ - 9
| Действующее вещество | Торговые названия |
| Информация отсутствует | |
| |
|
| |
|
Роль гормона ангиотензина для работы сердечно-сосудистой системы неоднозначна и во многом зависит от рецепторов, с которыми он взаимодействует. Наиболее известно его влияние на рецепторы первого типа, которые вызывают сужение сосудов, возрастание кровяного давления, способствуют синтезу гормона альдостерона, что влияет на количество солей в крови и объем циркулирующей крови.
Образование ангиотензина (ангиотонин, гипертензин) происходит путем сложных преобразований. Предшественником гормона является белок ангиотензиноген, большую часть которого вырабатывает печень. Белок этот относится к серпинам, большинство которых тормозят (ингибируют) ферменты, расщепляющие пептидную связь между аминокислотами в белках. Но в отличие от многих из них, ангиотензиноген на другие белки такого влияния не имеет.
Выработка белка повышается под воздействием гормонов надпочечников (прежде всего, кортикостероидов), эстрогенов, тиреоидных гормонов щитовидной железы, а также ангиотензина II, в который этот белок впоследствии преобразуется. Делает ангиотензиноген это не сразу: сначала под воздействием ренина, которые вырабатывают артериолы почечных клубочков в ответ на понижение внутрипочечного давления, ангиотензиноген трансформируется в первую, неактивную форму гормона.
Затем на него оказывает влияние ангиотензин превращающий фермент (АПФ), что образуется в лёгких и отщепляет от него две последние аминокислоты. В результате получается состоящий из восьми аминокислот активный октапептид, известный как ангиотонин II, который при взаимодействии с рецепторами оказывает влияние на сердечно-сосудистую, нервную системы, надпочечники и почки.
При этом гипертензин обладает не только сосудосуживающим действием и стимулирует выработку альдостерона, но и в больших количествах в одном из отделов головного мозга, гипоталамусе, повышает синтез вазопрессина, который влияет на выведение воды почками, способствует появлению чувства жажды.
Рецепторы гормона
В настоящий момент обнаружено несколько типов рецепторов ангиотонина II. Лучше всего изучены рецепторы подтипа АТ1 и АТ2. Большинство воздействий на организм как позитивных, так и негативных, происходит при взаимодействии гормона с рецепторами первого подтипа. Находятся они во многих тканях, больше всего – в гладких мышцах сердца, сосудов, в почках.
Влияют на сужение мелких артерий почечных клубочков, вызывая возрастание давления в них, способствуют реабсорбации (обратному всасыванию) натрия в почечных канальцах. От них во многом зависит синтез вазопрессина, альдостерона, эндотелина-1, работа адреналина и норадреналина, они же принимают участие в освобождение ренина.
К негативным воздействиям относят:
- угнетение апоптоза – апоптозом называют регулируемый процесс, во время которого организм избавляется от ненужных или поврежденных клеток, в том числе от злокачественных. Ангиотонин при влиянии на рецепторы первого типа способен притормозить их распад в клетках аорты и коронарных сосудов;
- увеличение количества «плохого холестерина», который способен спровоцировать атеросклероз;
- стимуляция разрастания гладкомышечных стенок сосудов;
- увеличение риска образования тромбов, которые замедляют ток крови по сосудам;
- гиперплазия интимы – утолщение внутренней оболочки кровеносных сосудов;
- активизация процессов ремоделирования сердца и сосудов, которая выражается в способности органа изменять свою структуру из-за патологических процессов, является одним из факторов артериальной гипертензии.

 Так, при слишком активной деятельности ренин-ангиотензиновой системы, которая регулирует давление и объем крови в организме, рецепторы АТ1 оказывают прямое и косвенное воздействие на повышение артериального давления. Также они негативно влияют на сердечно-сосудистую систему, вызывая утолщение стенок артерий, увеличение миокарда и другие недуги.
Так, при слишком активной деятельности ренин-ангиотензиновой системы, которая регулирует давление и объем крови в организме, рецепторы АТ1 оказывают прямое и косвенное воздействие на повышение артериального давления. Также они негативно влияют на сердечно-сосудистую систему, вызывая утолщение стенок артерий, увеличение миокарда и другие недуги.
Рецепторы второго подтипа также распространены по всему организму, больше всего находятся в клетках плода, после рождения их количество начинает уменьшаться. Некоторые исследования позволили предположить, что они оказывают существенное влияние на развитие и рост клеток эмбриона, формируют исследовательское поведение.
Доказано, что число рецепторов второго подтипа может возрастать при повреждении сосудов и других тканей, сердечной недостаточности, инфаркте. Это позволило выдвинуть предположение, что АТ2 участвуют в регенерации клеток и, в отличие от АТ1, способствуют апоптозу (гибели поврежденных клеток).
Исходя из этого, исследователи выдвинули предположение, что эффекты, которые оказывает ангиотонин через рецепторы второго подтипа, прямо противоположны его воздействию на организм через АТ1-рецепторы. В результате стимуляции АТ2 происходит вазодилатация (расширение просвета артерий и других кровеносных сосудов), тормозится увеличение мышечных стенок сердца. Воздействие этих рецепторов на организм находится лишь на стадии изучения, поэтому их влияние мало изучено.


Также почти неизвестна реакция организма на рецепторы третьего типа, которые были обнаружены на стенках нейронов, а также на АТ4, что расположены на эндотелиальных клетках, и отвечают за расширение и восстановление сети кровеносных сосудов, рост тканей и заживление при повреждениях. Также рецепторы четвертого подвида были найдены на стенках нейронов, и согласно предположениям отвечают за познавательные функции.
Разработки ученых в медикаментозной сфере
В результате многолетних исследований ренин-ангиотензиновой системы было создано немало лекарств, действие которых направлено на целенаправленное воздействие на отдельные части этой системы. Особое внимание ученые уделили негативному воздействию на организм рецепторов первого подтипа, что оказывают большое влияние на развитие сердечно-сосудистых осложнений, и поставили задачу разработать лекарства, направленные на блокирование этих рецепторов. Поскольку стало очевидно, что таким образом можно лечить артериальную гипертонию и предупредить сердечно-сосудистые осложнения.
В ходе разработок стало очевидно, что блокаторы рецепторов ангиотензина более эффективны, чем ингибиторы ангиотензин превращающего фермента, поскольку действуют сразу в нескольких направлениях и способны просачиваться сквозь гематоэнцефалический барьер.
Он разделяет центрально-нервную и кровеносную системы, защищая нервную ткань от находящихся в крови патогенов, токсинов, а также клеток иммунной системы, что из-за сбоев идентифицируют мозг как инородную ткань. Также он является барьером для некоторых лекарств, направленных на терапию нервной системы (зато пропускает питательные и биоактивные элементы).
Блокаторы рецепторов ангиотензина, проникнув сквозь барьер, притормаживают медиаторные процессы, что происходят в симпатической нервной системе. В результате угнетается высвобождение норадреналина и уменьшается стимуляция адреналиновых рецепторов, что находятся в гладких мышцах сосудов. Это приводит к возрастанию просвета кровеносных сосудов.
При этом каждый препарат обладает своими особенностями, например, такое влияние на организм особенно сильно выражено у эпроссартана, тогда как воздействие других блокаторов на симпатическую нервную систему противоречивы.

 Таким методом лекарства блокируют развитие эффектов, которые гормон оказывает на организм через рецепторы первого подтипа, предупреждая негативное воздействие ангиотонина на сосудистый тонус, способствуя обратному развитию гипертрофии левого желудочка и уменьшая слишком высокое артериальное давление. Регулярный продолжительный прием ингибиторов вызывает снижение гипертрофии кардиомиоцитов, разрастания гладкомышечных клеток сосудов, мезангиальных клеток и т.д.
Таким методом лекарства блокируют развитие эффектов, которые гормон оказывает на организм через рецепторы первого подтипа, предупреждая негативное воздействие ангиотонина на сосудистый тонус, способствуя обратному развитию гипертрофии левого желудочка и уменьшая слишком высокое артериальное давление. Регулярный продолжительный прием ингибиторов вызывает снижение гипертрофии кардиомиоцитов, разрастания гладкомышечных клеток сосудов, мезангиальных клеток и т.д.
Также необходимо заметить, что все антагонисты рецепторов ангиотензина характеризуются избирательным действием, которое направленно именно на то, чтобы блокировать рецепторы первого подтипа: на них они воздействуют в тысячи раз сильнее, чем на АТ2. Причем разница во влиянии для лозартана превышает тысячу раз, валсартана – двадцать тысяч раз.
При повышенной концентрации ангиотензина, что сопровождается блокадой АТ1-рецепторов, начинают проявляться защитные свойства гормона. Выражаются они в стимуляции рецепторов второго подтипа, что приводит к увеличению просвета кровеносных сосудов, замедление разрастания клеток и др.
Также при повышенном количестве ангиотензинов первого и второго типа образуется ангиотонин-(1-7), который также обладает сосудорасширяющим и натрийуретическим действиями. На организм он влияет через неидентифицированные АТх рецепторы.
Виды лекарств
Антагонисты рецепторов ангиотензина принято делить по химическому составу, фармакологическим характеристикам, способу связывания с рецепторами. Если говорить о химической структуре, ингибиторы принято делить на следующие виды:
- бифениловые производные тетразола (лозартан);
- бифениловые нететразоловые соединения (телмисартан);
- небифениловые нететразоловые соединения (эпросартан).
Что касается фармакологической активности, то ингибиторы могут являть собой активные лекарственные формы, которые характеризуются фармакологической активностью (валсартан). Или же быть пролекарствами, которые активизируются после преобразования в печени (кандесартана цилексетил). Некоторые ингибиторы содержат активные метаболиты (продукты обмена веществ), присутствие которых характеризуется более сильным и длительным воздействием на организм.


По механизму связывания препараты делят на такие, что обратимо связываются с рецепторами (лозартан, эпросартан), то есть при определенных ситуациях, например, когда происходит возрастание количества ангитензина в ответ на снижение циркулирующей крови, ингибиторы могут быть вытесненными из мест связывания. Есть и такие лекарства, что связываются с рецепторами необратимо.
Особенности приема препаратов
Больному назначают прием ингибиторов рецепторов ангиотензина при наличии артериальной гипертензии как при слабой, так и тяжелой форме недуга. Повысить эффективность блокаторов способно их сочетание с тиазидными диуретиками, поэтому уже разработаны препараты, что содержат в себе комбинацию этих лекарств.
Антогонисты рецепторов не являются препаратами быстрого действия, на организм они воздействуют плавно, постепенно, эффект держится около суток. При регулярной терапии выраженный лечебный эффект можно увидеть через две, и даже шесть недель после начала терапии. Принимать их можно вне зависимости от приема пищи, для эффективного лечения достаточно раз в день.
Препараты хорошо воздействуют на больных вне зависимости от пола и возраста, в т. ч. и на пожилых пациентов. Организм хорошо переносит все виды этих лекарств, что дает возможность использовать их для лечения больных с уже обнаруженной сердечно-сосудистой патологией.
Блокаторы рецепторов АТ1 имеют противопоказания и предостережения. Они запрещены людям с индивидуальной непереносимостью компонентов лекарства, беременным женщинам и в период лактации: они могут вызвать патологические изменения в организме малыша, результатом чего является его смерть в утробе матери или после рождения (это было установлено в ходе экспериментов над животными). Также не рекомендуют применять эти лекарства для лечения детей: насколько препараты для них безопасны, на сегодняшний день не определено.
С осторожностью врачи назначают ингибиторы людям, которые имеют пониженный объем циркулирующей крови, или анализы показали пониженное количество натрия в крови. Это обычно бывает при терапии диуретиками, если человек находится на бессолевой диете, при диарее. С оглядкой нужно применять препарат при аортальном или митральном стенозе, обструктивной гипертрофической кардиомиопатии.
Нежелателен прием лекарства людям, что находятся на гемодиализе (метод внепочечного очищения крови при почечной недостаточности). Если лечение назначают на фоне почечного заболевания, необходим постоянный контроль концентрации калия и крептинина сыворотки. Неэффективен препарат, если анализы показали повышенное количество альдостерона в крови.
Ангиотензин (АТ) - это гормон из рода олигопептидов, который отвечает за сужение сосудов и подъем АД в организме. Вещество является частью ренин-ангиотензиновой системы, регулирующей вазоконстрикцию. Кроме того, олигопептид активирует синтез альдостерона - гормона надпочечников. Альдостерон также способствует повышению давления. Прекурсором ангиотензина считается белок ангиотензиноген, вырабатываемый печенью.
Ангиотензин был выделен как самостоятельное вещество и синтезирован в 30-х годах прошлого столетия в Аргентине и Швейцарии.
Коротко об ангиотензиногене
Ангиотензиноген является ярким представителем класса глобулинов и имеет в своем составе более чем 450 аминокислот. Белок вырабатывается и высвобождается в кровь и лимфу постоянно. Его уровень в течение дня может меняться.

Повышение концентрации глобулина происходит под действием глюкокортикоидов, эстрогена и тиреодных гормонов. Этим объясняется стойкое повышение АД при использовании оральных контрацептивов на основе эстрогенов.
Если давление крови понижается, и содержание Na+ резко падает, происходит рост уровня ренина и скорость выработки ангиотензиногена значительно возрастает.
Количество этого вещества в плазме здорового человека составляет примерно один ммоль/л. При развитии гипертонии ангиотензиноген в крови повышается. При этом наблюдаются периоды рениновой активности, что выражается концентрацией ангиотензина 1 (АТ 1).
Под влиянием ренина, синтезируемого в почках, из ангиотензиногена образуется АТ 1. Элемент биологически неактивен, его единственное предназначение - быть прекурсором АТ 2, который формируется в процессе отщепления двух последних атомов с C-конца молекулы неактивного гормона.

Именно ангиотензин 2 является главным гормоном РААС (ренин-ангиотензин-альдостероновой системы). Он обладает выраженной сосудосуживающей активностью, задерживает в организме соль и воду, повышает ОПСС и АД.
Можно условно выделить два главных эффекта, которые ангиотензин II оказывает на больного:
- Пролиферативный. Проявляется увеличением объёма и массы кардиомиоцитов, соединительной ткани организма, клеток артериол, что вызывает уменьшение свободного просвета. Происходит неконтролируемое разрастание внутренней слизистой оболочки почки, увеличение количества мезангиальных клеток.
- Гемодинамический. Эффект проявляется в быстром повышении АД и системной вазоконстрикции. Сужение диаметра кровеносных сосудов происходит на уровне почечных артериол, в результате чего увеличивается давление крови в капиллярах.
Под воздействием ангиотензина II повышается уровень альдостерона, который задерживает в организме натрий и выводит калий, что провоцирует хроническую гипокалиемию. На фоне этого процесса снижается активность мышц, формируется стойкая гипертония.
Количество АТ 2 в плазме возрастает при следующих недомоганиях:
- рак почки, выделяющий ренин;
- нефротический синдром;
- почечная гипертония.

Уровень активного ангиотензина может быть и снижен. Это происходит при развитии таких заболеваний:
- острая почечная недостаточность;
- синдром Кона.
К снижению концентрации гормона может привести удаление почки.
Ангиотензин III и IV
В конце 70-х прошлого столетия был синтезирован ангиотензин 3. Гормон образуется при дальнейшем расщеплении эффекторного пептида до 7 аминокислот.
Ангиотензин III обладает меньшим сосудосуживающим эффектом, чем АТ 2, но при этом более активен в отношении альдостерона. Поднимает среднее АД.
Под действием ферментов аминопептидазы АТ III расщепляется до 6 аминокислот и образует ангиотензин IV. Он менее активен, чем АТ III и участвует в процессе гемостаза.

Основная функция активного олигопептида заключается в поддержке постоянного объема крови в организме. Ангиотензин влияет на процесс посредством АТ-рецепторов. Они бывают разных видов: АТ1-, АТ2-, АТ3-, АТ4-рецепторы и другие. Эффекты ангиотензина зависят от его взаимодействия с этими белками.
Наиболее близки по своему строению АТ 2 и АТ1-рецепторы, поэтому активный гормон в первую очередь соединяется с АТ1-рецепторами. В результате этой связи поднимается АД.
Если при высокой активности АТ 2 свободных АТ1-рецепторов нет, олигопептид соединяется с АТ 2-рецепторами. к которым менее предрасположен. В итоге запускаются антагонистические процессы, и АД понижается.
Ангиотензин II может влиять на организм как за счет непосредственного действия на клетки артериол, так и косвенного - через центральную или симпатическую нервную систему, гипоталамус и надпочечники. Его воздействие распространяется на концевые артерии, капилляры и венулы по всему организму.

Сердечно-сосудистая система
АТ 2 оказывает направленное вазоконстрикторное действие. Кроме сосудосуживающего эффекта, ангиотензин ii меняет силу сокращения сердца. Работая через ЦНС, гормон сдвигает симпатическую и парасимпатическую активность.
Влияние АТ 2 на организм в целом и сердечно-сосудистую систему в частности может быть преходящим или длительным.
Кратковременный эффект выражается вазоконстрикцией и стимуляцией выработки альдостерона. Продолжительное воздействие определяется тканевым АТ2, образующимся в эндотелии сосудистых областей сердечной мышцы.
Активный пептид провоцирует увеличение объёма и массы миокарда и нарушает метаболизм. Кроме того, он поднимает сопротивление в артериях, что провоцирует растяжение сосудов.
В результате воздействие ангиотензина II на сердечно-сосудистую систему развивается гипертрофия левого желудочка миокарда и стенок артерий, внутриклубочковая гипертензия.
ЦНС и головной мозг
АТ 2 оказывает опосредственное влияние на нервную систему и головной мозг через гипофиз и гипоталамус. Олигопептид стимулирует выработку АКТГ в передней части гипофиза и активирует синтез вазопрессина гипоталамусом.
Адиуретин, в свою очередь, оказывает яркое антидиуретическое действие, которое порождает:
- Задержку воды в организме, повышая обратное всасывание жидкости из полости почечных канальцев в кровь. Это способствует увеличению объема циркулирующей в организме крови и ее разжижению.
- Усиливает сосудосуживающий эффект ангиотензина II и катехоламинов.
АКТГ стимулирует надпочечники и повышает выработку глюкокортикоидов, из которых самым биологически активным является кортизол. Гормон, хотя он и не обладает вазоконстрикторным воздействием, усиливает сосудосуживающее влияние катехоламинов, секретируемых надпочечниками.

При резком повышении синтеза вазопрессина и АКТГ у больных появляется чувство жажды. Этому способствует и высвобождение норадреналина при прямом воздействии на симпатическую НС.
Надпочечники
Под влиянием ангиотензина в надпочечниках активируется высвобождение адольстерона. В результате происходит:
- задержка воды в организме;
- увеличение количества циркулирующей крови;
- рост частоты сокращений миокарда;
- усиление сосудосуживающего действия АТ 2.
Все эти процессы суммарно приводят к повышению АД. Эффект от чрезмерного уровня альдостерона можно наблюдать в период лютеиновой фазы месячного цикла у женщин.
Почки
В нормальных условиях ангиотензин II на функцию почек практически не влияет. Патологический процесс разворачивается на фоне чрезмерной активности РААС. Резкое уменьшение кровотока в тканях почки приводит к ишемии канальцев, затрудняет фильтрацию.
Процесс реабсорбции, вызывающий уменьшения количества мочи и выведение из организма натрия, калия и свободной жидкости, нередко приводит к обезвоживанию и появлению протеинурии.

Для кратковременного влияния АТ 2 на почки характерно повышение внутриклубочкового давления. При продолжительном воздействии развивается гипертрофия мезангиума.
К чему приводит функциональная активность ангиотензина II
Кратковременное повышение уровня гормона не оказывает на организм выраженного отрицательного воздействия. Совсем по-другому отражается на человеке длительное увеличение АТ 2. Оно нередко порождает целый ряд патологических изменений:
- Гипертрофию миокарда, кардиосклероз, сердечную недостаточность, инфаркт. Эти недуги возникают на фоне истощения сердечной мышцы, переходящей в миокардиодистрофию.
- Утолщение стенок сосудов и уменьшение просвета. В результате усиливается артериальное сопротивление и поднимается АД.
- Ухудшается кровоснабжение тканей организма, развивается кислородное голодание. В первую очередь от плохого кровообращения страдают мозг, миокард и почки. Постепенно формируется дистрофия этих органов, погибшие клетки замещаются фиброзной тканью, что еще больше усугубляет симптомы недостаточности кровообращения. Ухудшается память, появляются частые головные боли.
- Развивается инсулинорезистентность (пониженная чувствительность) к инсулину, что провоцирует обострение сахарного диабета.

Продолжительная активность олигопептидного гормона приводит к стойкому повышению АД, которое поддается только медикаментозному воздействию.
Норма ангиотензина I и II
Для определения уровня эффекторного пептида проводится анализ крови, ничем не отличающийся от обычного исследования на гормоны.
У больных артериальной гипертонией исследование выявляет активность ренина в плазме. На анализ берется кровь из вены после восьмичасового ночного сна и бессолевой диеты в течение 3 суток.
Как видно, ангиотензин II играет огромную роль в регуляции АД в организме. Следует настороженно относиться к любым изменениям уровня АТ 2 в крови. Конечно, это не означает, что при небольшом излишке гормона АД сразу поднимется до 220 мм рт. ст., а ЧСС - до 180 сокращений в минуту. По своей сути, олигопептидный гормон не может непосредственно повышать давление и провоцировать развитие гипертонии, но, тем не менее, он всегда активно участвует в формировании болезни.
Для цитирования:
Сидоренко Б.А., Преображенский Д.В., Заикина Н.В. ФАРМАКОТЕРАПИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ. Часть VI. Блокаторы ангиотензиновых рецепторов I типа как антигипертензивные препараты // РМЖ. 1998. №24. С. 4
Рассмотрены физиология ренин-ангиотензиновой системы и роль ее повышенной активности в патогенезе гипертонической болезни. Представлена сравнительная характеристика блокаторов ангиотензиновых рецепторов I типа.
The paper considers the physiology of the renin-angiotensin system and the role of its increased activity in the pathogenesis of essential hypertension. It comparatively characterizes antihypertensive angiotensin I receptor antagonists.
Б.А. Сидоренко, Д.В. Преображенский,
Н.В. Заикина - Медицинский центр Управления делами Президента Российской Федерации, Москва
V. A. Sidorenko, D. V. Preobrazhensky,
N. V. Zaikina - Medical Center, Administration of Affairs of the President of the Russian Federation, Moscow
Часть VI. Блокаторы ангиотензиновых рецепторов I типа как антигипертензивные препараты
Повышенная активность ренин-ангиотензиновой системы (РАС) в кровяном русле и тканях, как известно, является важным фактором патогенеза гипертонической болезни (ГБ) и некоторых вторичных форм артериальной гипертензии. Высокая активность ренина в плазме крови, отражающая гиперактивность РАС, является прогностически неблагоприятным показателем при ГБ. Так, у больных ГБ с высокой активностью ренина в плазме риск развития инфаркта миокарда в 3,8 раза выше, чем у больных с низкой активностью ренина. Высокая активность ренина в плазме крови сочетается с увеличением вероятности развития сердечно-сосудистых осложнений в 2,4 раза и смертности от всех причин - в 2,8 раза . До недавнего времени для подавления чрезмерной активности РАС у больных ГБ использовались симпатолитические средства центрального действия (резерпин), агонисты центральных a 2 -адренорецепторов (метилдопа, клонидин), b -адреноблокаторы (пропранолол, атенолол, метопролол и др.) и ингибиторы ангиотензинпревращающего фермента (АПФ). В 90-е годы появилась новая группа высокоэффективных антигипертензивных препаратов, действие которых основано на торможении активности РАС на уровне ангиотензиновых рецепторов I типа (АТ 1 -рецепторов) для ангиотензина II. Эти препараты получили название блокаторы АТ 1 -рецепторов, или антагонисты рецепторов для ангиотензина II.
Физиология ренин-ангиотензиновой системы
Для лучшего понимания механизмов антигипертензивного действия блокаторов АТ 1 -рецепторов необходимо остановиться на молекулярных и функциональных аспектах РАС.
Главным эффекторным пептидом РАС является ангиотензин II, который образуется из неактивного ангиотензина I под действием АПФ и некоторых других сериновых протеаз. Действие ангиотензина II на клеточном уровне опосредуется двумя типами мембранных рецепторов - АТ
1 и АТ 2 . Почти все известные физиологические (сердечно-сосудистые и нейроэндокринные) эффекты ангиотензина II опосредуются АТ
1 -рецепторами. Например, при ГБ имеют важное значение такие опосредуемые АТ
1 -рецепторами эффекты ангиотензина II, как артериальная вазоконстрикция и секреция альдостерона, а также стимуляция пролиферации кардиомиоцитов и гладкомышечных клеток сосудистой стенки. Все эти эффекты ангиотензина II, как полагают, способствуют повышению артериального давления (АД), развитию гипертрофии левого желудочка и утолщению стенок артерий, которое сопровождается уменьшением их просвета, у больных ГБ.
Таблица 1. Физиологические эффекты ангиотензина II, которые опосредуются АТ1- и АТ2-рецепторами (по C. Johnston и J. Risvanis)
| АТ 1 -рецепторы | АТ 2 -рецепторы |
| Вазоконстрикция | Стимуляция апоптоза |
| Стимуляция синтеза и секреции альдостерона | Антипролиферативный эффект |
| Реабсорбция натрия в почечных канальцах | Дифференцировка и развитие эмбриональных тканей |
| Гипертрофия кардиомиоцитов | Рост эндотелиальных клеток |
| Пролиферация гладкомышечных клеток сосудистой стенки | Вазодилатация |
| Усиление периферической норадреналинергической активности | |
| Усиление активности центрального звена симпатической | |
| нервной системы | |
| Стимуляция высвобождения вазопрессина | |
| Снижение почечного кровотока | |
| Торможение секреции ренина |
Эффекты ангиотензина II, опосредуемые АТ 2 -рецепторами, стали известны лишь в последние годы. При ГБ наиболее важное значение имеют те физиологические эффекты ангиотензина II (а также ангиотензина III), которые опосредуются АТ
2 -рецепторами, а именно вазодилатация и торможение пролиферации клеток, в том числе кардиомиоцитов, фибробластов и гладкомышечных клеток сосудистой стенки (табл. 1). Как можно видеть, при стимуляции АТ
2 -рецепторов ангиотензин II частично ослабляет свои собственные эффекты, связанные со стимуляцией АТ
1 -рецепторов.
Схема 1. Пути образования двух основных эффекторных пептидов РАС - ангиотензина II и ангиотензина-(I-7). Ангиотензин II в дальнейшем превращается в ангиотензин III и ангиотензин IV, обладающие некоторой биологической активностью, которая опосредуется соответственно АТ 3 - и АТ 4 -рецепторами (на схеме не обозначены).
АТ 1 -рецепторы на мембранах гепатоцитов и клеток юкстагломерулярного аппарата (ЮГА) почек опосредуют механизмы отрицательной обратной связи в РАС. Поэтому в условиях блокады АТ
1 -рецепторов в результате нарушений этих механизмов отрицательной обратной связи увеличиваются синтез ангиотензиногена в печени и секреция ренина клетками ЮГА почек. Иными словами, при блокаде АТ
1 -рецепторов происходит реактивная активация РАС, которая проявляется повышением уровня ангиотензиногена, ренина, а также ангиотензина I и ангиотензина II.
Повышенное образование ангиотензина II в условиях блокады АТ
1 -рецепторов приводит к тому, что начинают преобладать эффекты ангиотензина II, опосредуемые АТ 2 -рецепторами. Следовательно, последствия блокады АТ
1 -рецепторов двоякие. Прямые последствия связаны с ослаблением фармакологических эффектов, опосредуемых АТ 1 -рецепторами. Косвенные последствия являются результатом стимуляции АТ
2 -рецепторов ангиотензином II, который в условиях блокады АТ
1 -рецепторов образуется в повышенном количестве.
Третий механизм антигипертензивного действия блокаторов АТ
1 -рецепторов объясняется повышенным образованием в условиях блокады АТ
1 -рецепторов другого эффекторного пептида РАС - ангиотензина-(I-7), обладающего вазодилатирующими свойствами. Ангиотензин-(I-7) образуется из ангиотензина I под действием нейтральной эндопептидазы и из ангиотензина II под действием пролиловой эндопептидазы. В условиях блокады АТ
1 -рецепторов повышенный уровень ангиотензина I и ангиотензина II в крови предрасполагает к усиленному превращению их в ангиотензин-(I-7) .
Ангиотензин-(I-7) обладает вазодилатирующим действием и натрийуретическими свойствами, которые опосредуются простагландинами I2, кининами и оксидом азота. Эти эффекты ангиотензина-(I-7) обусловлены его действием на неидентифицированные пока АТ-рецепторы - АТх-рецепторы (схема 1).
Таким образом, механизмов антигипертензивного действия у блокаторов АТ
1 -рецепторов три - один прямой и два косвенных. Прямой механизм связан с ослаблением эффектов ангиотензина II, которые опосредуются АТ
1 -рецепторами. Косвенные механизмы связаны с реактивной активацией РАС в условиях блокады АТ
1 -рецепторов, которая ведет к повышенному образованию как ангиотензина II, так и ангиотензина-(I-7). Ангиотензин II оказывает антигипертензивное действие, стимулируя незаблокированные АТ
2 -рецепторы, в то время как ангиотензин-(I-7) оказывает антигипертензивное действие, стимулируя АТх-рецепторы (схема 2).
Клиническая фармакология блокаторов АТ 1 -рецепторов
Существуют два основных типа АТ-рецепторов - АТ 1 и АТ
2 . Соответственно различают селективные блокаторы АТ
1 - и АТ
2 -рецепторов. В клинической практике используются блокаторы АТ
1 -рецепторов, которые оказывают антигипертензивное действие. В настоящее время применяются или проходят клинические испытания по меньшей мере восемь непептидных селективных блокаторов АТ
1 -рецепторов: вальзартан, золарзартан, ирбезартан, кандезартан, лозартан, тазозартан, тельмизартан и эпрозартан.
По химической структуре непептидные блокаторы АТ
1 -рецепторов можно разделить на три основные группы:
. бифениловые производные тетразола - лозартан, ирбезартан, кандезартан и др.;
. небифениловые производные тетразола - эпрозартан и др.;
. негетероциклические соединения - вальзартан и др. .
Некоторые блокаторы АТ
1 -рецепторов сами по себе обладают фармакологической активностью (вальзартан, ирбезартан), другие (например, кандезартана цилексетил) становятся активными лишь после ряда метаболических превращений в печени. Наконец, у таких активных АТ
1 -блокаторов, как лозартан и тазозартан, есть активные метаболиты, оказывающие более сильное и длительное действие, чем сами препараты. Следовательно, блокаторы АТ
1 -рецепторы можно разделить на активные препараты и пролекарственные формы АТ
1 -блокаторов.
По механизму связывания с АТ
1 -рецепторами доступные АТ
1 -блокаторы разделяются на конкурентные и неконкурентные антагонисты ангиотензина II. К конкурентным АТ 1 -блокаторам относятся вальзартан, ирбезартан и лозартан, к неконкурентным - активная форма кандезартана цилексетила (кандезартан) и активный метаболит лозартана (Е-3174).
Продолжительность антигипертензивного действия блокаторов АТ
1 -рецепторов определяется как прочностью их связи с АТ
1 -рецепторами, так и периодом полужизни препаратов или их активных лекарственных форм и активных метаболитов (табл. 2).
Наряду с блокаторами АТ 1 -рецепторов существуют селективные блокаторы АТ
2 -рецепторов - CGP 42112 и PD 123319. В отличие от АТ
1 -блокаторов блокаторы АТ
2 -рецепторов не оказывают антигипертензивного действия и пока не используются в клинической практике.
Лозартан
- первый непептидный блокатор АТ 1 -рецепторов, который успешно прошел клинические испытания и разрешен к использованию для лечения ГБ и хронической сердечной недостаточности.
После приема внутрь лозартан всасывается в желудочно-кишечном тракте; концентрация препарата в плазме крови достигает максимума в течение 30 - 60 мин. При первом прохождении через печень лозартан в значительной степени метаболизируется, в результате чего его системная биодоступность составляет 19 - 62% (в среднем 33%). Период полужизни лозартана в плазме крови составляет 2,1 ± 0,5 ч. Тем не менее антигипертензивный эффект препарата сохраняется на протяжении 24 ч, что объясняется наличием у него активного метаболита - Е-3174, который в 10 - 40 раз сильнее блокирует АТ
1 -рецепторы, чем лозартан. Кроме того, у Е-3174 более длительный период полужизни в плазме крови - от 4 до 9 ч. Лозартан и Е-3174 выводятся из организма как через почки, так и через печень. Через почки выводится примерно 50% всего количества Е-3174.
Рекомендуемая доза лозартана при лечении артериальной гипертензии - 50 - 100 мг/сут в один прием .
Вальзартан
- высокоселективный блокатор АТ 1 -рецепторов. Он более селективен, чем лозартан. В то время как у лозартана сродство к АТ
1 -рецепторам в 10 000 раз выше, чем к АТ
2 -рецепторам, у вальзартана показатель АТ
1 -селективности составляет 20 000 - 30 000: 1. У вальзартана в отличие от лозартана нет активных метаболитов. Период его полужизни в плазме крови составляет около 5 - 7 ч и сопоставим с таковым активного метаболита лозартана Е-3174. Это объясняет, почему антигипертензивный эффект вальзартана сохраняется в течение 24 ч. Основной путь элиминации вальзартана - выведение с желчью и калом.
Больным ГБ вальзартан назначают в дозе 80 - 160 мг/сут в один прием .
Ирбезартан
- селективный блокатор АТ
1 -рецепторов. Как АТ
1 -блокатор он менее селективен, чем вальзартан. Показатель АТ
1 -селективности у ирбезартана такой же, как у лозартана - 10 000: 1. Ирбезартан в 10 раз сильнее связывается с АТ
1 -рецепторами, чем лозартан, и несколько сильнее, чем активный метаболит лозартана Е-3174.
Биодоступность ирбезартана составляет 60 - 80%, что значительно выше, чем у других блокаторов АТ
1 -рецепторов.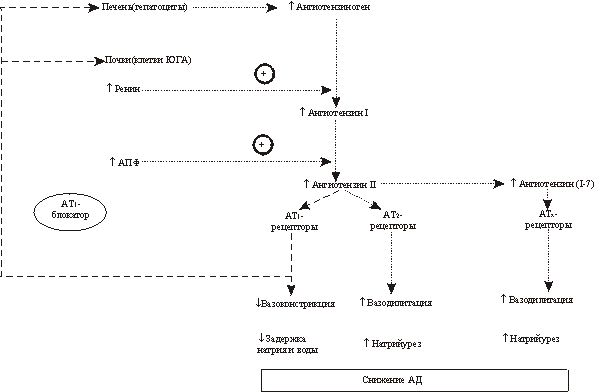
Схема 2. Прямые и косвенные последствия блокады АТ 1 -рецепторов. Снижение АД при лечении селективными блокаторами АТ 1 -рецепторов является следствием не только ослабления эффектов ангиотензина II, опосредуемых АТ 1 -рецепторами, но и усиления эффектов ангиотензина II, опосредуемых АТ 2 -рецепторами, и эффектов ангиотензина-(I-7), опосредуемых АТ х -рецепторами.
В отличие от лозартана и вальзартана биодоступность ирбезартана не зависит от совместного приема пищи. Период полужизни ирбезартана в плазме крови достигает 11 - 17 ч. Ирбезартан выводится из организма преимущественно с желчью и калом; с мочой выводится примерно 20% дозы препарата.
Для лечения ГБ ирбезартан назначают в дозе 75 - 300 мг/сут в один прием .
Кандезартана цилексетил
- пролекарственная форма АТ 1 -блокатора. После приема внутрь кандезартана цилексетила в крови не обнаруживается, поскольку быстро и полностью превращается в активное соединение - кандезартан (CV-11974). Сродство кандезартана к АТ
1 -рецепторам более чем в 10 000 раз выше, чем сродство к АТ
2 -рецепторам. Кандезартан в 80 раз сильнее связывается с АТ
1 -рецепторами, чем лозартан, и в 10 раз сильнее, чем активный метаболит лозартана Е-3174.
Кандезартан прочно связывается с АТ
1 -рецепторами, диссоциация его из связи с АТ 1 -рецепторами происходит медленно. Эти данные о кинетике связывания кандезартана с АТ
1 -рецепторами дают основание предполагать, что в отличие от лозартана кандезартан действует как неконкурентный антагонист ангиотензина II.
После приема кандезартана цилексетила максимальная концентрация его активной формы - кандезартана - в плазме крови обнаруживается через 3,5 - 6 ч. Период полужизни кандезартана в плазме крови колеблется от 7,7 до 12,9 ч, составляя в среднем 9 ч. Из организма кандезартан выводится через почки, а также с желчью и калом.
Средняя доза кандезартана цилексетила для лечения артериальной гипертензии - 8 - 16 мг/сут в один прием .
Эпрозартан
- селективный блокатор АТ 1 -рецепторов. По химической структуре он отличается от других АТ
1 -блокаторов тем, что является небифениловым производным тетразола. Эпрозартан обладает важным дополнительным свойством: он блокирует пресинаптические АТ
1 -рецепторы в симпатической нервной системе. Благодаря этому свойству эпрозартан (в отличие от вальзартана, ирбезартана и лозартана) тормозит высвобождение норадреналина из окончаний симпатических нервных волокон и тем самым уменьшает стимуляцию a1-адренорецепторов гладкой мускулатуры сосудов. Иными словами, у эпрозартана имеется дополнительный механизм вазодилатирующего действия. Кроме того, эпрозартан, и вальзартан в отличие от лозартана и ирбезартана не оказывают влияния на активность ферментов цитохромной Р-450 системы и не взаимодействует с другими лекарственными препаратами.
Таблица 2. Сравнительная характеристика основных блокаторов АТ1-рецепторов
| Препарат | Биодоступность, % | Активный метаболит |
Период полужизни, ч |
|
| препарата | активного метаболита | |||
| Вальзартан | 10 - 35 | Нет | 5 - 7 | - |
| Ирбезартан | 60 - 80 | Нет | 11 - 17 | - |
| Кандезартана цилексетил | ? | Кандезартан | 3,5 - 4 | 8 - 13 |
| Лозартан | 19 - 62 | Е-3174 | 1,5 - 2 | 4 - 9 |
| Эпрозартан | 13 | Нет | 5 - 9 | - |
Эпрозартан является активной формой блокатора АТ 1 -рецепторов. Его биодоступность при приеме внутрь составляет около 13%. Концентрация эпрозартана в плазме крови достигает максимума в течение 1 - 2 ч после приема препарата внутрь. Период полужизни эпрозартана в плазме крови составляет 5 - 9 ч. Эпрозартан выводится из организма в основном с желчью и калом в неизмененном виде; примерно 37% принятой внутрь дозы препарата экскретируется с мочой.
Для лечения артериальной гипертензии эпрозартан назначают в дозе 600 - 800 мг/сут в один или два приема .
Таблица 3. Основные сердечно-сосудистые и нейроэндокринные эффекты блокаторов АТ1-рецепторов
| . Сердечно-сосудистые (и почечные) эффекты:
Системная артериальная вазодилатация (снижение АД, уменьшение общего периферического сосудистого сопротивления и посленагрузки на левый желудочек);
Нейроэндокринные эффекты: Повышение уровня ангиотензина II, ангиотензина I и активности ренина в плазме; |
Фармакологические эффекты блокаторов АТ
1
-рецепторов
По механизму действия блокаторы АТ
1 -рецепторов во многом напоминают ингибиторы АПФ. Блокаторы АТ 1 -рецепторов и ингибиторы АПФ подавляют чрезмерную активность РАС, действуя на различные уровни этой системы. Поэтому фармакологические эффекты АТ
1 -блокаторов и ингибиторов АПФ в общем сходны, однако первые, будучи более избирательными ингибиторами РАС, значительно реже дают побочные эффекты.
Основные сердечно-сосудистые и нейроэндокринные эффекты блокаторов АТ
1 -рецепторов приведены в табл. 3.
Показания и противопоказания к назначению АТ
1 -блокаторов также во многом совпадают с таковыми для ингибиторов АПФ. Блокаторы АТ
1 -рецепторов предназначены для длительной терапии ГБ и хронической сердечной недостаточности. Перспективным, как полагают, может оказаться применение АТ
1 -блокаторов при лечении диабетической нефропатии и других поражений почек, включая реноваскулярную гипертензию.
Противопоказаниями
к назначению блокаторов АТ
1 -рецепторов считаются: индивидуальная непереносимость препарата, беременность, грудное вскармливание. Требуется большая осторожность при назначении блокаторов АТ
1 -рецепторов при стенозирующем поражении обеих почечных артерий или артерии единственной функционирующей почки.
Опыт применения блокаторов АТ 1 -рецепторов при лечении ГБ
В последние годы блокаторы АТ 1 -рецепторов находят все более широкое применение в качестве антигипертензивных средств. Это объясняется тем, что АТ
1 -блокаторы сочетают высокую антигипертензивную эффективность с превосходной переносимостью. Кроме того, блокаторы АТ
1 -рецепторов дают клинически значимый протективный эффект. Они способны вызывать обратное развитие гипертрофии левого желудочка и подавлять гипертрофию гладкой мускулатуры сосудистой стенки, уменьшают внутриклубочковую гипертензию и протеинурию. В сердце и почках АТ
1 -блокаторы ослабляют развитие фиброзных изменений.
В большинстве случаев блокаторы АТ
1 -рецепторов оказывают значительное и равномерное антигипертензивное действие, которое сохраняется до 24 ч. Поэтому все доступные АТ 1 -блокаторы рекомендуется принимать один раз в сутки. Если антигипертензивный эффект блокатора АТ
1 -рецепторов недостаточен, добавляют диуретик.
Лозартан был первым блокатором АТ
1 -рецепторов, который стал использоваться для лечения ГБ. По данным литературы , лозартан в дозе 50 - 100 мг/сут снижает систолическое АД в среднем на 10 - 20%, диастолическое - на 6 - 18%. Антигипертензивная эффективность лозартана сравнима с таковой эналаприла, атенолола и фелодипина-ретард и значительно превосходит эффективность каптоприла.
Опыт клинического изучения эффективности и безопасности лозартана почти у 3000 больных ГБ свидетельствует, что побочные эффекты при его применении встречаются с такой же частотой, как и при назначении плацебо (соответственно 15,3 и 15,5%).
В отличие от ингибиторов АПФ лозартан и другие АТ 1 -рецепторов не вызывают мучительного сухого кашля и ангионевротического отека. Поэтому АТ
1 -блокаторы, как правило, рекомендуют использовать для лечения артериальной гипертензии у больных с противопоказаниями к назначению ингибиторов АПФ.
Лозартан - единственный АТ
1 -блокатор, о котором известно, что он способен увеличивать продолжительность жизни больных с хронической сердечной недостаточностью в большей степени, чем ингибитор АПФ каптоприл . Учитывая данные о профилактической эффективности лозартана при хронической сердечной недостаточности, все блокаторы АТ
1 -рецепторов рекомендуется использовать в качестве антигипертензивных препаратов первого ряда для лечения артериальной гипертензии у больных с систолической дисфункцией левого желудочка.
Вальзартан назначают в дозе 80 - 160 мг/сут. В дозе 160 мг/сут вальзартан, по-видимому, более эффективен как антигипертензивный препарат, чем лозартан в дозе 1
00 мг/сут. Как и другие АТ
1 -блокаторы, вальзартан отличается превосходной переносимостью. Частота побочных эффектов при его длительном применении не отличается от таковой при назначении плацебо (соответственно 15,7 и 14,5%) .
Ирбезартан назначают в дозе 150 - 300 мг/сут. В дозе 300 мг/сут препарат более эффективен, чем лозартан в дозе 100 мг/сут. Частота побочных эффектов при лечении ирбезартаном и назначении плацебо одинакова .
Кандезартана цилексетил, по-видимому, самый сильный из доступных в
настоящее время блокаторов АТ 1 -рецепторов. Его назначают в дозе 4 - 16 мг/сут. В дозе 16 мг/сут кандезартан в значительно большей степени снижает АД, чем лозартан в дозе 50 мг/сут. Кандезартан, по-видимому, оказывает более продолжительное антигипертензивное действие, чем лозартан. Кандезартан превосходно переносится больными. Из-за развития побочных эффектов препарат пришлось отменить у 1,6 - 2,2% больных ГБ против 2,6% больных, получавших плацебо .
Эпрозартан назначают в дозе 600 и 800 мг/сут в
один прием. При тяжелой гипертензии эпрозартан и эналаприл в одинаковой степени снижали диастолическое АД (в среднем соответственно на 20,1 и 16,2 мм рт. ст.), однако эпрозартан вызывал достоверно большее снижение систолического АД, чем эналаприл (в среднем соответственно на 29,1 и 21,1 мм рт. ст.). Частота побочных эффектов при назначении эпрозартана такая же, как при приеме плацебо.
Таким образом, блокаторы АТ 1 -рецепторов представляют собой новый класс антигипертензивных препаратов. Антигипертензивная эффективность АТ
1 -блокаторов сопоставима с таковой ингибиторов АПФ при гораздо лучшей переносимости.
Литература:
1. Alderman MN, Ooi WL, Madhavan S, et al. Plasma renin activity: A risk factor for myocardial infection in hypertensive patients. Amer
J Hypertens 1997;10:1-8.
2. Johnston CI, Risvanis J. Preclinical pharmacology of angiotensin II receptor anta-
gonists. Amer J Hypertens 997;10:306S-310S.
3. Преображенский Д.В., Сидоренко Б.А., Соколова Ю.В., Носова И.К. Физиология и фармакология ренин-ангиотензиновой системы. Кардиология 1997;11:91-5.
4. Bauer JH, Reams GP. The angiotensin II type receptor antagonists. Arch Intern Med 1955;155:1361-8.
5. Сидоренко Б.А., Преображенский Д.В., Соколова Ю.В. Лозартан - первый представитель нового класса гипотензивных препаратов. Кардиология 1996;1:84-9.
6. Goa KL, Wagstaff A. Losartan potassium. A review of its pharmacology. Drugs 1996;51:820-45.
7. McIntyre M, Caffe SE, Machalar RA, Reid JL. Losartan, an orally active angiotensin (AT
1) receptor antagonist: A review of its efficacy and safety in essential hypertension. Pharmacol Ther 1997;74:181-94.
8. Markham A, Goa KL. Valsartan. A review of its pharmacology and therapeutic use in essential hypertension. Drugs 1997;54:299-311.
9. Brunner HR. The new angiotensin II receptor antagonist, irbesartan. Pharmacokinentec and pharmacodynamic considerations. Amer J Hypertens 1997;10:311S-317S.
10. Nishikawa K, Naka T, Chatani F, Ioshimure I. Candesartan cilexetil: A review of its preclinic
al pharmacology. J Hum Hypertens 1997;11(suppl 2):9-17.
11. Edwards RM, Aiyar N, Ohlstein EH, et al. Pharmacological characterization of non-peptide angiotensin II receptor antagonist, SK&F 108566. J Pharmacol Exp Ther 1992;260:175-81.
12. Сидоренко
Б.А., Носова И.К., Преображенский Д.В. Антагонисты АТ
1
-ангиотензиновых рецепторов - новая группа лекарственных препаратов для лечения артериальной гипертензии и хронической сердечной недостаточности. Клин. вестник 1997;4:26-8.
13. Pitt B, Segal R, Marti
nez FA, et al. Randomised trial of losartan versus captopril in patients over 65 with hert failure (Evaluation of Losartan in the Elderly study, ELITE). Lancet 1997;349:747-52.
14. Pool JL, Gutlirie RM, Littlejohn TW, et al. Dose-related antihypertensive effects of irbesartan in patients with mild-to-moderate hypertension. Amer J Hypertens 1998;11:462-70.
15. Andersson OK, Neldam S. The antihypertensive effect and tolerability of candesartan cilexetil, a new generation angiotensin II antagonist, in co
mparison with losartan. Blood Pressure 1998;7:53-9.
16. Belcher G, HЯbner R, George M, et al. Candesartan cilexetil: safety and tolerability in healthy volunteers and patients with hypertension. J Hum Hypertens 1997;11(suppl 2):85-9.
Ангиотензин – это пептидный гормон, который вызывает сужение кровеносных сосудов (вазоконстрикцию), повышение артериального давления, а также высвобождение альдостерона из коры надпочечников в кровеносное русло.
Ангиотензин играет значимую роль в ренин-ангиотензин-альдостероновой системе, которая является главной целью лекарственных средств, снижающих артериальное давление.
Основной механизм действия антагонистов рецепторов ангиотензина 2 связан с блокадой АТ 1 -рецепторов, за счет чего устраняется неблагоприятное воздействие ангиотензина 2 на тонус сосудов и нормализуется повышенное артериальное давление.
Уровень ангиотензина в крови повышается при почечной гипертензии и новообразованиях почек, продуцирующих ренин, а понижается при обезвоживании организма, синдроме Конна и удалении почки.
Синтез ангиотензина
Предшественником ангиотензина является ангиотензиноген – белок класса глобулинов, который относится к серпинам и вырабатывается преимущественно печенью.
Выработка ангиотензина 1 происходит под влиянием на ангиотензиноген ренина. Ренин – протеолитический фермент, который относится к наиболее значимым почечным факторам, принимающим участие в регуляции артериального давления, при этом сам он прессорными свойствами не обладает. Ангиотензин 1 также не обладает вазопрессорной активностью и быстро превращается в ангиотензин 2, который является наиболее мощным из всех известных прессорных факторов. Превращение ангиотензина 1 в ангиотензин 2 происходит за счет удаления С-концевых остатков под воздействием ангиотензинпревращающего фермента, который присутствует во всех тканях организма, однако больше всего синтезируется в легких. Последующее расщепление ангиотензина 2 обусловливает образование ангиотензина 3 и ангиотензина 4.
Помимо этого, способностью образовывать ангиотензин 2 из ангиотензина 1 обладают тонин, химазы, катепсин G и другие сериновые протеазы, что является так называемым альтернативным путем образования ангиотензина 2.
Ренин-ангиотензин-альдостероновая система
Ренин-ангиотензин-альдостероновая система – это гормональная система, которая обеспечивает регуляцию артериального давления и объема циркулирующей в организме крови.
Лекарственные средства, действующие путем блокады ангиотензиновых рецепторов, были созданы в ходе изучения ингибиторов ангиотензина 2, которые способны блокировать его образование или действие и таким образом снижать активность ренин-ангиотензин-альдостероновой системы.
Ренин-ангиотензин-альдостероновый каскад начинается с синтеза препроренина путем трансляции рениновой мРНК в юкстагломерулярных клетках афферентных артериол почек, где из препроренина, в свою очередь, образуется проренин. Значительная часть последнего путем экзоцитоза выбрасывается в кровоток, однако часть проренина превращается в ренин в секреторных гранулах юкстагломерулярных клеток, затем также выделяясь в кровеносное русло. По этой причине в норме объем циркулирующего в крови проренина значительно выше концентрации активного ренина. Контроль выработки ренина является определяющим фактором активности ренин-ангиотензин-альдостероновой системы.
Ренин регулирует синтез ангиотензина 1, не обладающего биологической активностью и выступающего прекурсором ангиотензина 2, служащего сильным вазоконстриктором прямого действия. Под его влиянием происходит сужение кровеносных сосудов и последующее повышение кровяного давления. Также он имеет протромботический эффект – регулирует адгезию и агрегацию тромбоцитов. Кроме того, ангиотензин 2 потенциирует высвобождение норадреналина , повышает выработку адренокортикотропного гормона и антидиуретического гормона, способен вызывать чувство жажды. За счет повышения давления в почках и сужения эфферентных артериол ангиотензин 2 увеличивает скорость гломерулярной фильтрации.

Ангиотензин 2 оказывает свое действие на клетки организма через рецепторы ангиотензина (АТ-рецепторы) разных типов. Наибольшее сродство ангиотензин 2 имеет к АТ 1 -рецепторам, которые локализуются преимущественно в гладкой мускулатуре кровеносных сосудов, сердце, некоторых областях мозга, печени, почках, коре надпочечников. Период полураспада ангиотензина 2 составляет 12 минут. Ангиотензин 3, формирующийся из ангиотензина 2, обладает 40% его активности. Период полураспада ангиотензина 3 в кровотоке составляет примерно 30 секунд, в тканях организма – 15–30 минут. Ангиотензин 4 является гексопептидом и схож по своим свойствам с ангиотензином 3.
Продолжительное повышение концентрации ангиотензина 2 приводит к уменьшению чувствительности клеток к инсулину с высоким риском развития сахарного диабета второго типа.
Ангиотензин 2 и внеклеточный уровень ионов калия относятся к наиболее значимым регуляторам альдостерона, который является важным регулятором баланса калия и натрия в организме и играет значимую роль в контроле объема жидкостей. Он увеличивает реабсорбцию воды и натрия в дистальных извитых канальцах, собирательных трубках, слюнных и потовых железах, толстом кишечнике, вызывая экскрецию ионов калия и водорода. Повышенная концентрация альдостерона в крови приводит к задержке в организме натрия и усиленному выделению калия с мочой, то есть к снижению уровня данного микроэлемента в сыворотке крови (гипокалиемия).
Повышенный уровень ангиотензина
При длительном увеличении концентрации ангиотензина 2 в крови и тканях повышается образование коллагеновых волокон и развивается гипертрофия гладкомышечных клеток кровеносных сосудов. В результате стенки кровеносных сосудов утолщаются, уменьшается их внутренний диаметр, что приводит к повышению артериального давления . Помимо этого, происходит истощение и дистрофия клеток сердечной мышцы с их последующей гибелью и замещением соединительной тканью, что является причиной развития сердечной недостаточности .
Длительный спазм и гипертрофия мышечного слоя кровеносных сосудов обусловливают ухудшение кровоснабжения органов и тканей, в первую очередь головного мозга, сердца, почек, зрительного анализатора. Продолжительный недостаток кровоснабжения почек приводит к их дистрофии, нефросклерозу и формированию почечной недостаточности. При недостаточном кровоснабжении головного мозга наблюдаются нарушения сна, эмоциональные расстройства, снижение интеллекта, памяти, шум в ушах, головная боль, головокружение и пр. Ишемия сердца может осложняться стенокардией , инфарктом миокарда . Недостаточное кровоснабжение сетчатки глаза приводит к прогрессирующему снижению остроты зрения.
Ренин регулирует синтез ангиотензина 1, не обладающего биологической активностью и выступающего прекурсором ангиотензина 2, служащего сильным вазоконстриктором прямого действия.
Продолжительное повышение концентрации ангиотензина 2 приводит к уменьшению чувствительности клеток к инсулину с высоким риском развития сахарного диабета второго типа.
Блокаторы ангиотензина 2
Блокаторы ангиотензина 2 (антагонисты ангиотензина 2) – это группа лекарственных средств, снижающих артериальное давление.
Лекарственные средства, действующие путем блокады ангиотензиновых рецепторов, были созданы в ходе изучения ингибиторов ангиотензина 2, которые способны блокировать его образование или действие и таким образом снижать активность ренин-ангиотензин-альдостероновой системы. К таким веществам относятся ингибиторы синтеза ринина, ингибиторы образования ангиотензиногена, ингибиторы ангиотензинпревращающего фермента, антагонисты ангиотензиновых рецепторов и пр.
Блокаторы (антагонисты) рецепторов ангиотензина 2 – это группа гипотензивных лекарственных средств, которая объединяет препараты, модулирующие функционирование ренин-ангиотензин-альдостероновой системы через взаимодействие с ангиотензиновыми рецепторами.

Основной механизм действия антагонистов рецепторов ангиотензина 2 связан с блокадой АТ 1 -рецепторов, за счет чего устраняется неблагоприятное воздействие ангиотензина 2 на тонус сосудов и нормализуется повышенное артериальное давление. Прием препаратов данной группы обеспечивает продолжительный антигипертензивный и органопротекторный эффект.
В настоящее время продолжаются клинические исследования, посвященные изучению эффективности и безопасности блокаторов рецепторов ангиотензина 2.
Видео с YouTube по теме статьи:
